薬の効き目や副作用に影響する
薬物代謝酵素の活性評価法を開発
薬が体にどのように作用するかには個人差がある。抗がん剤などの効果の強い薬では、よく効く人がいる一方で、強い副作用のために投与量を減らしたり、時には治療を中止せざるを得ない場合もある。こうした薬の効き目や副作用の個人差に大きく関わっているのが、薬物代謝酵素だ。
体内に取り込まれた薬物は、薬物代謝酵素によって分解され、体外に排出される。この酵素活性が低いと、副作用が強く出る危険性があり、一方活性が高いと、薬の効き目が悪くなることもある。「もし薬物治療を始める前に薬物代謝酵素活性が極めて低い人を見つけ出せたら、あらかじめ薬の投与量を最適化し、副作用のない治療が可能になります」。そう話す柴﨑浩美准教授は、こうした個別化医療への貢献を目指し、薬物代謝酵素の活性を評価する方法を研究している。
柴﨑准教授が注目しているのが、シトクロムP450 3A(CYP3A)という薬物代謝酵素だ。CYP3Aは、臨床で使用されている医薬品の実に半数の代謝に関与しており、とりわけ評価法の開発が急がれる重要な薬物代謝酵素の一つだ。「既存のCYP3A活性を評価する方法の多くは、プローブ薬物(テスト薬物)を用いた方法です。治療に関係ない薬物を投与する方法は患者の負担になるため、プローブ薬物を使わずに、もともと体にある(内因性)物質を用いた評価法も報告されていますが、いまだ実際に臨床で使われている方法はありません」と言う。
その中で柴﨑准教授は、内因性コルチゾールをバイオマーカーとしてCYP3A活性を評価する、これまでにない方法を開発している。それが、内因性コルチゾールの6β-水酸化代謝クリアランス(CLm(6β))を指標として、CYP3Aの活性を評価する方法だ。
内因性コルチゾールは、CYP3Aによって、6β-ヒドロキシコルチゾール(6β-OHF)に代謝される。柴﨑准教授は、「酵素の代謝活性を最も反映する指標は、その酵素が関与する『代謝クリアランス(血液から薬物が除去される速度)』である」とする先行研究に基づいて、コルチゾールがCYP3Aによって6β-OHFに代謝されるスピード(CLm(6β))からCYP3Aの活性を評価する方法を確立した。CLm(6β)は、代謝後の尿中の6β-OHFの量を、血中コルチゾール濃度と時間から算出される面積で割り算することで求められる。「この方法なら、プローブ薬物を投与せず、1回の採尿・採血でCYP3Aの活性を評価できます」
柴﨑准教授は、安定同位体標識コルチゾールを用いてこの評価法を検証し、内因性のCLm(6β)であっても、CYP3A活性を評価する指標になることを確かめた。また人を対象とした複数の実験で、CLm(6β)によってCYP3A活性を正しく評価できることも確認している。
1回の採血でCYP3A活性を評価する新しい方法を確立
「内因性コルチゾールの6β-水酸化代謝クリアランスを用いたCYP3Aの活性評価法を確立したものの、この方法は、尿と血液の両方を採取する必要があり、患者にとってはやや負担があります」と柴﨑准教授。そこで次はこの評価法をベースに、1回の採血のみでCYP3A活性を評価できる方法の開発を試みた。
考え出したのが、血中コルチゾールと6β-OHFの比で評価する方法だ。「これまでに血中の6β-OHF/コルチゾール比で評価した報告はほとんどありません」と言う。理由は、血液中の6β-OHF濃度は0.1~2.0ng/mLと極めて微量で、定量が難しいためだ。柴﨑准教授は、LC-MS/MS(液体クロマトグラフ-タンデム質量分析計)を使って、6β-OHFとコルチゾールを同時に定量することに成功。この血中6β-OHF/コルチゾール比が、先に確立したCLm(6β)と良好な相関関係を示すことを確認した。
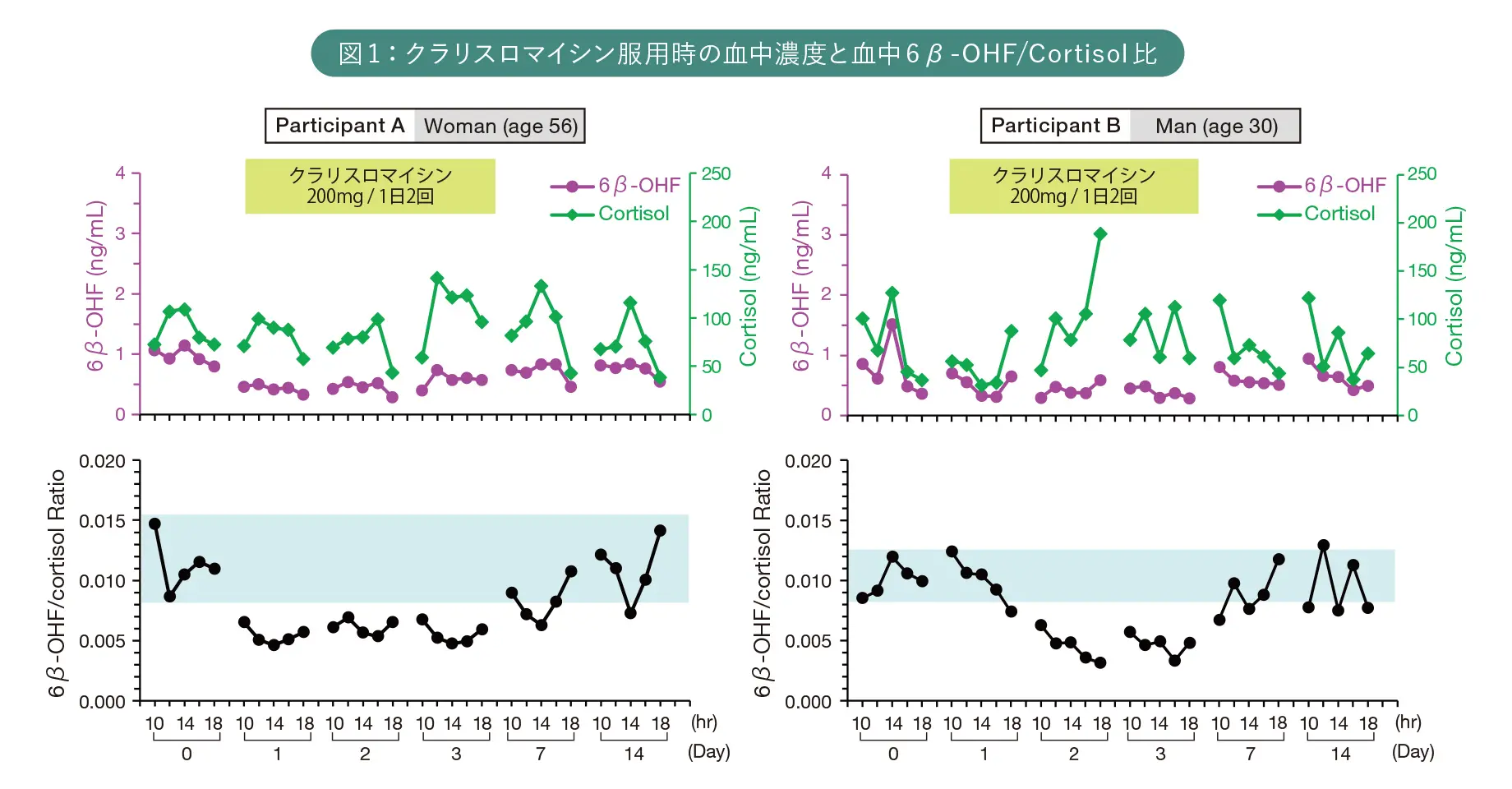
続いて柴﨑准教授は、血中6β-OHF/コルチゾール比は、CYP3A活性を評価する指標として有用であることを複数の実証実験で確認している。その一つとして、健康な女性を対象に、CYP3A阻害作用のある経口避妊薬の服用前・服用中・服用後の血中6β-OHF/コルチゾール比の経時変化を調べた。その結果、血中6β-OHF/コルチゾール比は、経口避妊薬服用21日後には39%–61%減少。CLm(6β)と同様の挙動を示し、CYP3A活性の変動を正確に捉えていることが確認された。またCYP3A阻害作用のあるクラリスロマイシンを1日2回連続服用した際の血中6β-OHF/コルチゾール比の経時変化を評価した結果でも、服用後4時間で37%、服用3日後には47%減少。CYP3A活性阻害を正確に把握できることが確かめられた[図1]。さらに健常な成人22名を対象に、性別による血中6β-OHF/コルチゾール比の差を調べた結果では、男性(0.0059-0.0116)に比べて、女性(0.0073-0.0172)の方が、活性がやや高いことが明らかになった。本学 臨床薬理学教室 田中祥子先生との共同研究では、CYP3Aで代謝される薬を投与された際に副作用を発現した2歳児の血中6β-OHF/コルチゾール比からCYP3A活性の評価を試みた。その結果、この2歳児のCYP3A活性は成人に比べてかなり低いことも確認した。現在はより幅広い対象でデータを蓄積し、基準範囲を設定するべく実証研究に取り組んでいる。
より簡便・低侵襲なCYP3A活性評価方法を探索
柴﨑准教授は、さらに簡便で低侵襲なCYP3A活性の評価方法を模索し、乾燥ろ紙血を試料として6β-OHFとコルチゾールを定量する方法も開発した。この方法なら、例えば僻地や離島など遠隔地で採取した試料を評価することも可能になる。現在は、より痛みを伴わずに採取できる唾液を用いた活性評価法の開発を進めている。
柴﨑准教授の開発したCYP3A活性評価法が臨床に応用されれば、副作用のない個別化医療につながる。さらにこの活性評価法は連続的な活性の変化を捉えられるため、医薬品開発の分野で、薬物を投与した時のCYP3A活性の経時変化の評価にも寄与できる。
安全で有効な薬物治療への貢献を目指し、柴﨑准教授と研究室メンバーの研究は続いていく。