延び続けるヒトの平均寿命と「最大寿命」
ヒトの寿命は、近年、著しく延びてきました。100歳以上の人はセンテナリアン(centenarian)とよばれますが、日本はその最多国です。日本におけるセンテナリアンは、1981年に1,000人を超え、1998年に1万人、2012年には5万人を超えました。そして、2025年9月現在は99,763人で、前年から4,644人増加しています(参考1)。今現在は、おそらく既に10万人を突破していることでしょう。日本のセンテナリアンの約88%が女性です。
日本の最高齢記録は、田中カ子(かね)さんの119歳107日(1903年-2022年)で、世界第2位にあたります。第1位は、フランスのジャンヌ・カルマンさんの122歳164日(1875年-1997年)です。
センテナリアンの数は、日本のみならず欧州をはじめ世界的に増加しています。では、それに伴って最高長寿記録が次々と更新されているかというと、必ずしもそうではありません。このことは、ヒトの寿命には環境要因だけでは説明しきれない生物学的な限界、すなわち種に固有の「最大寿命」が存在する可能性を示唆しています。
ニシオンデンザメの驚異的な寿命
哺乳類、あるいは恒温脊椎動物の中で最も長寿とされるのはホッキョククジラで、その最大寿命は200歳を超えるとされています(参考2)。一方、変温動物まで含めた脊椎動物全体で最も長寿が確認されているのは、ニシオンデンザメです。
北大西洋に生息するニシオンデンザメは、最大で全長7.3 mに達します。2016年、デンマークの研究グループは、グリーンランド周辺に生息するニシオンデンザメのうち体長502 cmの個体について、年齢を392±120歳と推定しました(参考3)。
この推定には、考古学でも用いられる放射性炭素年代測定が利用されました。多くの生体組織では新陳代謝によって分子が入れ替わりますが、眼の水晶体を構成するタンパク質は代謝されず、形成当初のものが生涯にわたって保持されます。自然界には放射性同位体である炭素14が一定の割合で存在し、半減期5,730年で崩壊します。この性質を利用して水晶体中の炭素14量を測定することで、生まれた年代を推定することが可能になります。
推定年齢392歳の個体は、日本でいえば江戸時代初期の生まれに相当します。誤差を考慮して最も若い推定値である272歳と見積もった場合でも、江戸時代中期の生まれにあたり、脊椎動物として確認されている中では最高水準の長寿記録です。
長寿ザメの視覚に関する新たな発見
ニシオンデンザメは、このように地球上で最も長寿の個体が確認されている脊椎動物です。その生息域は北大西洋から北極海にかけての深海であり、氷点下の低水温や高水圧といった過酷な環境に適応しています。
一方で、多くの個体では、眼球に寄生するカイアシ類(甲殻類の仲間)によって視界が妨げられている可能性があります。さらに、極端な暗闇の環境や数百年にも及ぶ寿命を踏まえると、このサメが視覚能力を失っている可能性も指摘されてきました。
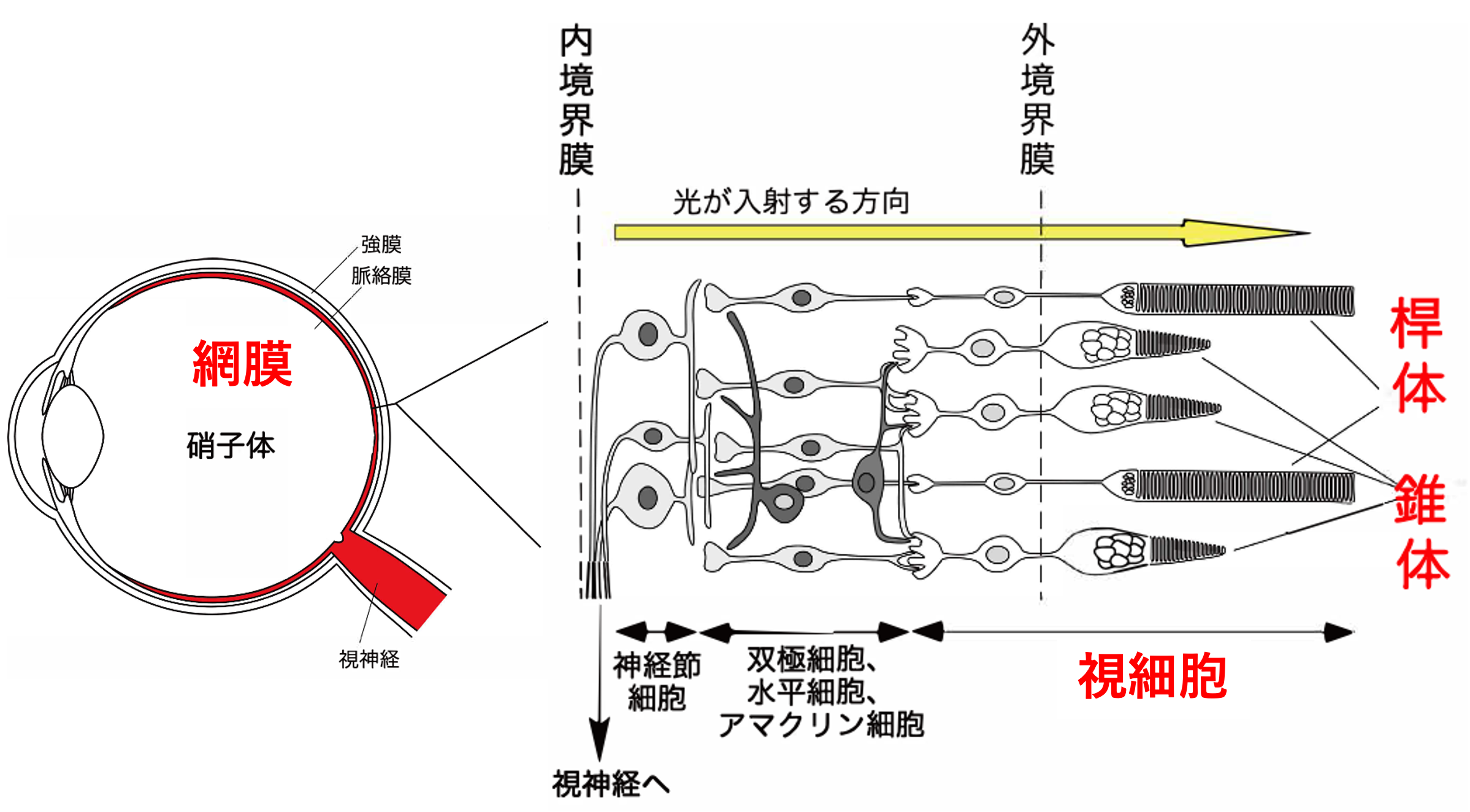
一般に脊椎動物の視覚は、暗所視に適した桿体細胞と、明所視を担う錐体細胞によって成り立っています(図)。これらの視細胞の構成や感受性は、生息環境に応じて進化してきました。深海生物や夜行性動物では桿体が優勢となり、場合によっては錐体が完全に失われることもあります。さらに、恒常的な暗闇に適応した種では、視覚そのものが退化する例も知られています。
こうした背景から、ニシオンデンザメは視力喪失の可能性が考えられてきました。しかし近年、行動観察や脳構造の比較研究から、視覚を完全には失っていない可能性が示唆されています。
2026年1月に『Nature Communications』誌に掲載された論文では、このサメの視覚について、ゲノム解析、遺伝子発現解析、組織学的手法、分光学的解析を組み合わせた包括的な検討が行われました(参考4)。
その結果、100歳を超える成体でも網膜に明らかな変性は認められず、機能的な視覚系が保持されていることが示されました。この視覚系は極めて低照度の環境に適応しており、さらに、DNA修復機構が網膜の完全性維持に重要な役割を果たしている可能性が示唆されています。
長寿ザメの視覚研究からヒトへ
ヒトの平均寿命は、日本をはじめ世界的に延び続けています。それに伴ってセンテナリアンの数も増加しています。長寿社会を考えるうえで重要なのは、「どれだけ長く生きるか」だけでなく、「どのように生きるか」という視点、すなわち生活の質(QOL)の維持です。
加齢に伴う視力や聴力などの感覚機能の低下は、生活の質や自立度に大きな影響を与えます。とくに視覚は主要な情報入力経路であり、その衰えは社会的孤立や認知機能の低下とも関連します。
加齢に関連する眼疾患としては、老眼(調節力の低下)や白内障(水晶体が白濁)、加齢黄斑変性(網膜の障害)、緑内障(眼圧の上昇などによる視神経障害)などが挙げられます。なかでも加齢黄斑変性をはじめとする網膜疾患は、進行性で修復が困難な損傷によって生じます。
その点で、ニシオンデンザメが数世紀にわたって網膜神経細胞と網膜機能を維持している事実は、きわめて注目に値します。
なぜこのサメの網膜は、長期にわたって構造と機能を保ち続けることができるのでしょうか。その答えはまだ明らかではありませんが、代謝の低さやDNA修復機構の持続的な働きなど、複数の要因が関与していると考えられます。この生物学的な仕組みを解明することは、ヒトの加齢性視力低下の予防に向けた新たな手がかりとなる可能性があります。
長寿動物の研究から老化の再考へ
従来、ヒトの老化研究は、寿命延長そのものに主な関心が向けられてきました。しかし近年では、加齢に伴う機能低下をいかに抑え、健康な状態をより長く維持するか、すなわち「健康寿命」の延伸に関心が移っています。
その意味で、ニシオンデンザメのように数世紀にわたって神経組織や感覚機能を維持する生物の存在は、老化に伴う機能喪失の予防に対しても重要な示唆を与えます。
こうした長寿動物の研究は、ヒトの老化を理解するための新たな視点を提供するとともに、「老いるとは何か」という根源的な問いを、あらためて私たちに投げかけます。
参考文献
- 厚生労働省.報道発表資料「令和7年度 百歳の高齢者へのお祝い状及び記念品の贈呈について」.2025年9月12日.
- Firsanov D, et al. Evidence for improved DNA repair in the long-lived bowhead whale. Nature, 648, 717–725 (2025).
- Nielsen J, et al. Eye lens radiocarbon reveals centuries of longevity in the Greenland shark (Somniosus microcephalus). Science, 353, 702–704 (2016).
- Fogg L. G., et al. The visual system of the longest-living vertebrate, the Greenland shark. Nature Communications, 17, 39 (2026).
※ 図はhttps://bsd.neuroinf.jp/w/images/2/21/Tachibanaki_Fig1.png より作成しました