2024年のノーベル生理学・医学賞が、10月7日に発表されました(参考1)。受賞するのは米国マサチューセッツ大学のビクター・アンブロス博士とマサチューセッツ総合病院・ハーバード大学のゲイリー・ラブカン博士、授賞理由は「マイクロRNAの発見と転写後遺伝子制御における役割」です。この報を聞き、シドニー・ブレナー(1927〜2019)が開いた道の広がりを、改めて感じました。
アンブロスとラブカンの発見
1980年代後半、アンブロスとラブカンは、ともにマサチューセッツ工科大学のロバート・ホロビッツの研究室で、博士研究員として線虫を用いた研究をしていました。さまざまなタイプの細胞が適切な時期に発生します。その遺伝プログラムが活性化するタイミングを制御する遺伝子に興味をもち、lin-4やlin-14という突然変異株を研究しました。二人は、博士研究員を終えてそれぞれの研究室をもちましたが、1989年にホロビッツやジョン・サルストン(後述)らとの共著でlin-14に関する論文を発表しました(参考2)。また、アンブロスは、lin-4遺伝子がlin-14遺伝子を負に制御することを明らかにしました(参考3)。
アンブロスとラブカンは、lin-4がどのようにlin-14の活性を阻害するかを研究しました。そして、今回の受賞のきっかけとなった二つの論文(参考4,5)に至ります。論文は、1993年にCell誌に同時に掲載されました。
アンブロスらは、驚くべきことに、lin-4遺伝子は異常に短いRNA分子を生成し、タンパク質生成のためのコードを欠いていることを見出しました(参考4)。これは、受賞理由の前半(マイクロRNAの発見)に相当します。ラブカンは、lin-4が制御するのはlin-14遺伝子からのmRNAの産生ではなくその後のタンパク質産生であり、それによって種々の細胞が変化するタイミングを制御することを明らかにしました(参考5)。これは、受賞理由の後半(転写後遺伝子制御における役割)に相当します。
マイクロRNA(miRNA)による遺伝子制御の新しい原理が発見されたわけですが、当初は線虫特有の現象と考えられました。これを一変したのは、2000年にラブカンらが発表した別のmiRNAをコードするlet-7遺伝子でした(参考6)。let-7遺伝子は、lin-4とは異なって高度に保存され、ヒトを含め動物界全体に存在します(参考7)。
マイクロRNA(miRNA)とは
miRNAは、20~25塩基程度の一本鎖RNAです。メッセンジャーRNA(mRNA)と同様にゲノムにコードされていますが、タンパク質には翻訳されません。代表的な機能は、標的となるmRNAに結合してタンパク質合成を抑制することです。このmiRNAによる抑制的な遺伝子制御のメカニズムは数億年前から存在し、複雑な生物の進化を可能にする一因となったことが考えられます(参考1)。
ヒトでは、1000種類を超えるmiRNAが見つかっています。miRNAによる制御の異常は、癌の一因となる可能性があります。また、miRNAをコードする遺伝子の変異が先天性難聴や眼や骨格などの障害を引き起こすことが知られています。
線虫C.エレガンス(Caenorhabditis elegans)
アンブロスとラブカンの研究は、C.エレガンスという非寄生性の土壌線虫を用いて行われました。線虫は、線形動物門に分類される動物の総称です。正式に種として認められているものだけでも、約2万種類あります(参考8)。大半の種は土壌や海洋中で非寄生性の生活を営んでいますが、植物や動物に寄生する線虫も知られています。大村智の2015年ノーベル生理学・医学賞の受賞理由は、「線虫の寄生によって引き起こされる感染症に対する新たな治療法に関する発見」でした。
C.エレガンスの全長は1 mm程度で、実験室では通常、大腸菌を餌として20〜25℃で培養されています。最近、この線虫の習性(がん患者の尿に誘引され、健常者の尿を忌避する)を利用した検査方法がTV等で宣伝されています。しかし以前は、害も益も無く、一般には注目されない存在でした。にもかかわらず、2002、2006、2008年にノーベル賞がC. エレガンスを用いた研究に授与され、そして今回です。なぜ、C. エレガンスは、大きな研究成果を生む実験モデル生物となったのでしょうか? シドニー・ブレナーの先見の明がありました。
先駆者シドニー・ブレナー
ブレナーは、1927年に南アフリカで生まれました。6歳のときに、3学年飛び級をして小学校4年に入学しました。15歳のときに奨学金を得てヨハネスブルグにある大学に入学し、翌年に医学部に進みました。1952年に英国に渡り、オックスフォード大学の大学院生となりました(参考8)。
1953年、ブレナーは、ジェームス・ワトソンとフランシス・クリックがDNAの二重らせん構造を明らかにしたと聞き、ケンブリッジまで二人に会いに行きました。このとき、ブレナー26歳、ワトソン25歳、クリックは36歳です。その後、ブレナーは遺伝暗号の解読に取り組むようになりました。1954年に南アフリカに一旦帰国しますが、1957年、クリックがいる研究所で研究職につきました。分子生物学の夜明けの時代で、ブレナーはクリックとともにmRNAの概念の誕生に貢献し(参考9)、遺伝暗号が連続した3塩基からなることを1961年に明らかにしました(参考10)。
このようにブレナーは、分子生物学の黎明期に活躍した花形研究者の一人です。1963年、ブレナーは新たな研究提案を、ケンブリッジ医学研究審議会の長であるマックス・ペルーツに宛てた手紙に書いています(参考11)。その中で次のように述べています。「分子生物学の古典的な問題のほとんどは既に解明されたか、解明されつつある。分子生物学の将来は、生物学の他の分野、特に発生や神経系に研究を広げることである。」
ブレナーは、分子生物学が大きく発展した要因は、大腸菌とバクテリオファージ(細菌に感染して増殖するウィルス)、そして遺伝学を用いたことにあると考えました。そのことに倣い、多細胞生物を対象とする発生や神経系の研究も、大腸菌のように簡便に扱えて遺伝学を容易に用いることができる実験モデル生物が必要と考えました。ブレナーはさまざまな生物を検討しました。ショウジョウバエは複雑すぎて解析が難しいと考え、より簡単な生物を探しました。そして線虫に行きつき、最終的にC.エレガンスを選びました。
ブレナーは、C.エレガンスにおける遺伝学を確立すること、神経回路を明らかにすること、細胞系譜を明らかにして組織・器官の形成過程を目指しました。ブレナーの下には、サルストンやホロビッツらの若い研究者が集まりました。先に述べたように、アンブロスとラブカンは後のホロビッツの研究室で研究し、サルストンとも連名で論文(参考3)を発表しました。
線虫研究から生まれたノーベル賞
ブレナー、ホロビッツ、サルストンは、2002年のノーベル生理学・医学賞を受賞しました。受賞理由は、「器官発生とプログラム細胞死の遺伝制御に関する発見」です。ブレナーがC.エレガンスの遺伝学を樹立し、サルストンが全細胞の系譜とプログラム細胞死の存在を明らかにし、ホロビッツがプログラム細胞死の遺伝子とメカニズムを明らかにしました。プログラム細胞死は、発生や癌、免疫など、さまざまな領域で重要です。
2006年の生理学・医学賞は、「2本鎖RNAによる遺伝子発現抑制現象(RNA 干渉)の発見」で、アンドリュー・ファイアーとクレイグ・メローが受賞しました。ファイアーも、ブレナーがいるケンブリッジの研究所で研究をしたことがあります。RNA干渉はC.エレガンスで発見されました。これは、mRNAに対して相補的な配列をもつ一本鎖RNAが会合するとmRNAの分解が起こる現象です。哺乳細胞でもRNA干渉を起こせることが判明し、生命科学研究の進め方は革命的に変わりました。RNA干渉はmiRNAの作用とも関連する現象ですが、報告されたのは1998年で、miRNAが発見された当時はまだ知られていませんでした。
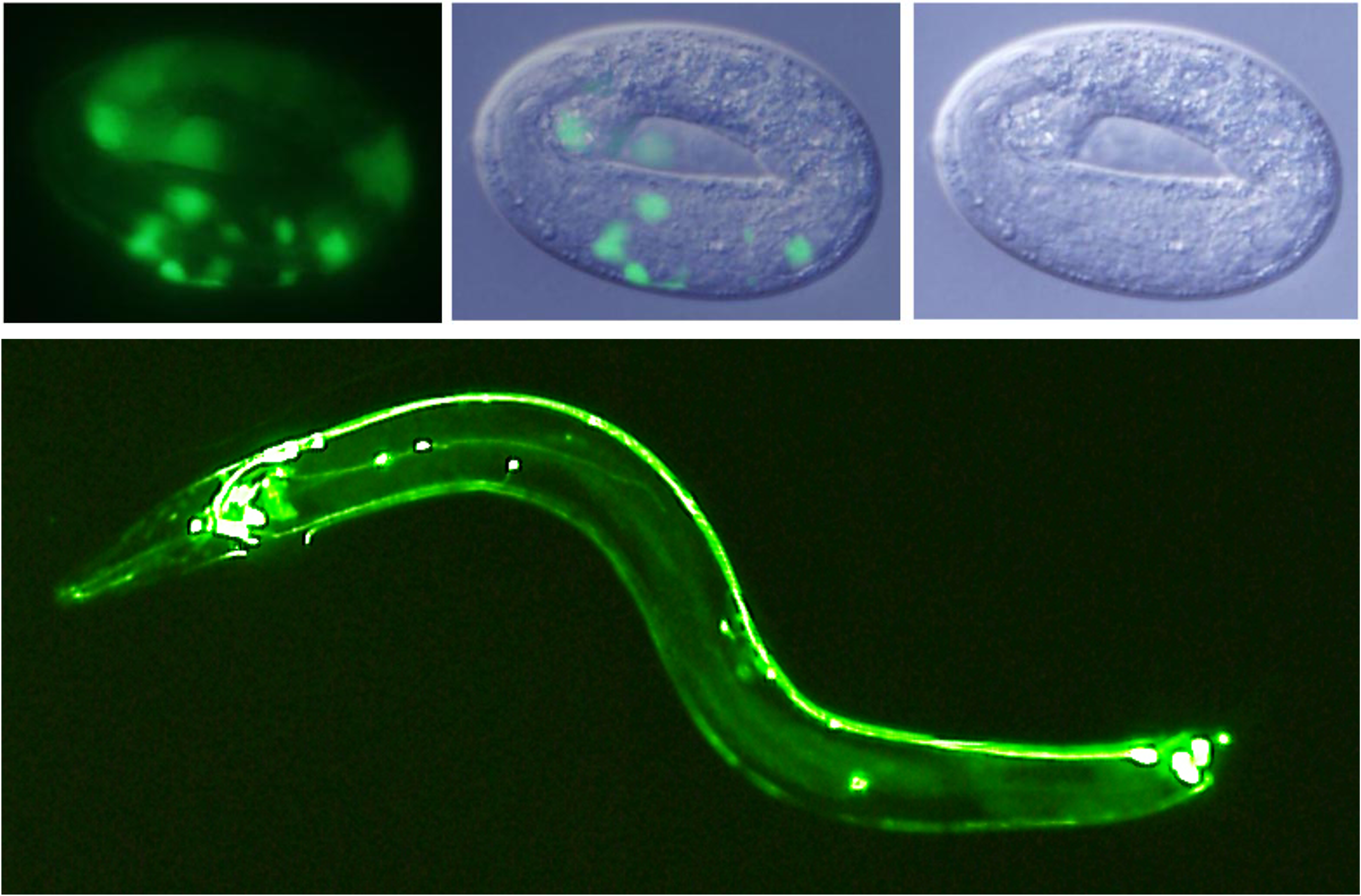
2008年は化学賞が、下村脩、マーティン・チャルフィー、ロジャー・Y・チエンの「緑色蛍光タンパク質(GFP)の発見と開発」に授与されました。チャルフィーもケンブリッジで研究をしたことがあります。チャルフィーは、GFPを多細胞生物として初めてC.エレガンスの体内で発現させ、研究ツールとして有用なことを示しました。C.エレガンスは透明なので、生きたままGFPの光を観察できます(写真)。GFPも、生命科学研究に革命的な影響をもたらしました。
ブレナーの先見が導いた大きな展開
分子生物学黎明期の花形研究者だったブレナーは、発生・神経系の研究へと舵を切り、C.エレガンスを用いることで道を開きました。そして、ブレナーのもとで育った研究者たち、さらに彼らの下で育った研究者たちが新たな野を拓いています。アンブロスとラブカンの業績も、そうした野の一つといえるでしょう。ブレナーが始めたことの波及の大きさを改めて思った、今回のノーベル生理学・医学賞でした。
【参考】
1. カロリンスカ研究所、プレスリリース、2024年10月7日、 https://www.nobelprize.org/prizes/medicine/2024/press-release/
2. Ruvkun Gら (1989) Molecular genetics of the Caenorhabditis elegans heterochronic gene lin-14. Genetics 121, 501-516.
3. Ambros V. (1989) A hierarchy of regulatory genes controls a larva-to-adult developmental switch in C. elegans. Cell 57, 49-57.
4. Lee RCら (1993) The C. elegans heterochronic gene lin-4 encodes small RNAs with antisense complementarity to lin-14. Cell 75, 843-854.
5. Wightman Bら (1993) Posttranscriptional regulation of the heterochronic gene lin-14 by lin-4 mediates temporal pattern formation in C. elegans. Cell 75, 855-862.
6. Reinhart BJら (2000) The 21-nucleotide let-7 RNA regulates developmental timing in Caenorhabditis elegans. Nature 403, 901-906.
7. Pasquinelli AEら (2000) Conservation of the sequence and temporal expression of let-7 heterochronic regulatory RNA. Nature 408, 86-89.
8. 大島靖美(2015) 線虫の研究とノーベル賞への道、裳華房.
9. Brenner Sら (1961) An unstable intermediate carrying information from genes to ribosomes for protein synthesis. Nature 190, 576-581.
10. Crick FHら (1961) General nature of the genetic code for proteins. Nature 192, 1227-1232.
11. Brenner S. (1988) The nematode Caenorhabditis elegans(Wood WB ら編), 序文, Cold Spring Harbor Laboratory.