生体の持つ光る原理を活用し生命現象を解き明かす
ヒトの体は数十兆もの細胞で構成されており、さらに小さなレベルで見ると、ナノサイズの分子の集まりである。「生命の営みとは、つきつめれば化学反応です。細胞の中で起こっていることを目で見ることはできませんが、分子の挙動や化学反応を追うことで、そのメカニズムを理解することが可能になる。こうした化学的な視点から生命現象を解き明かそうとするアプローチが、ケミカルバイオロジーという研究分野です」。そう解説した藤川雄太准教授は、この分野において、特に「光」を道具に使って生命現象を捉えようとしている。
「自然界には、発光する機能を備えた生物がたくさんいます。よく知られているように、ホタルはルシフェリンという発光分子を持っており、これがルシフェラーゼという酵素によって酸化されると、黄緑色の光を放ちます。生体の持つ光る原理は、標的の細胞や分子の働きを捉えるマーカーとして活用できます。ホタルのルシフェリンも生物学の研究ではなくてはならない分子なのです。」と言う。藤川准教授が焦点を当てている蛍光プローブは、特定の分子に特異的に反応・結合することで蛍光を発し、標的の物質を検出する。例えば多様な人工蛍光タンパクを創製し、ノーベル化学賞を受賞したRoger Y. Tsienが開発した蛍光プローブFura-2は、細胞内のカルシウムイオンを検出する手段としてよく知られている。
がん細胞に高発現するGSTP1を捉える蛍光プローブを開発
藤川准教授は、とりわけがんの性質を可視化できる蛍光プローブの開発に取り組んでいる。これまで焦点を当てているのが、GSTP1(Pi-class Glutathione S-Transferase)というタンパクだ。
GSTP1は、生体内で有害分子の解毒や薬物代謝を担うグルタチオンS-転移酵素(GST:Glutathione S-Transferase)の一種である。藤川准教授らは、このGSTP1活性に特異的に反応する蛍光プローブを開発。2019年、分析試薬CellFluorTM GSTP1(旧品名:GSTP1 Green)として商品化され、大きな話題を呼んだ。
「細胞内に入った異物分子は、GSTが触媒となってグルタチオンと結合し、グルタチオン抱合体に変換されます。形成されたグルタチオン抱合体はMRPトランスポーターによって速やかに細胞外に排出されます。これがGSTによる異物排除メカニズムです」と藤川准教授。原核生物から真核生物にまで多岐にわたって存在するGSTには多くの種類があり、中でもPiクラスとして知られるGSTP1は多くのがん細胞で高発現していることから、研究の現場で腫瘍マーカーとして活用されてきた。しかし薬物代謝酵素であるGSTは様々な基質(薬物や体内で生じる毒性分子など)を代謝するため、一般に基質特異性が低い。それゆえ、特定のGST(GSTP1)だけに特異的に反応する基質は見出されていなかったという。

藤川准教授らは、探索の末にGSTP1に選択的に反応する基質(2-ニトロ5-メシルベンズアニリド)を得ることに成功。この構造を組み込んだ蛍光プローブPs-TGをデザインし、合成した。「Ps-TGそのものは全く光りません。しかし、GSTP1活性によってグルタチオンが結合すると非常に強く光るようになることが分かりました」。しかしPs-TGには一つ大きな問題があった。水溶性が高く、細胞膜を透過しにくいため、細胞の中になかなか入れないのだ。そこで藤川准教授らはPs-TGが細胞の中に入れるように、Ps-TG分子内のフェノール性水酸基をアセチル化し分子の脂溶性を高めたPs-TAcを合成した。
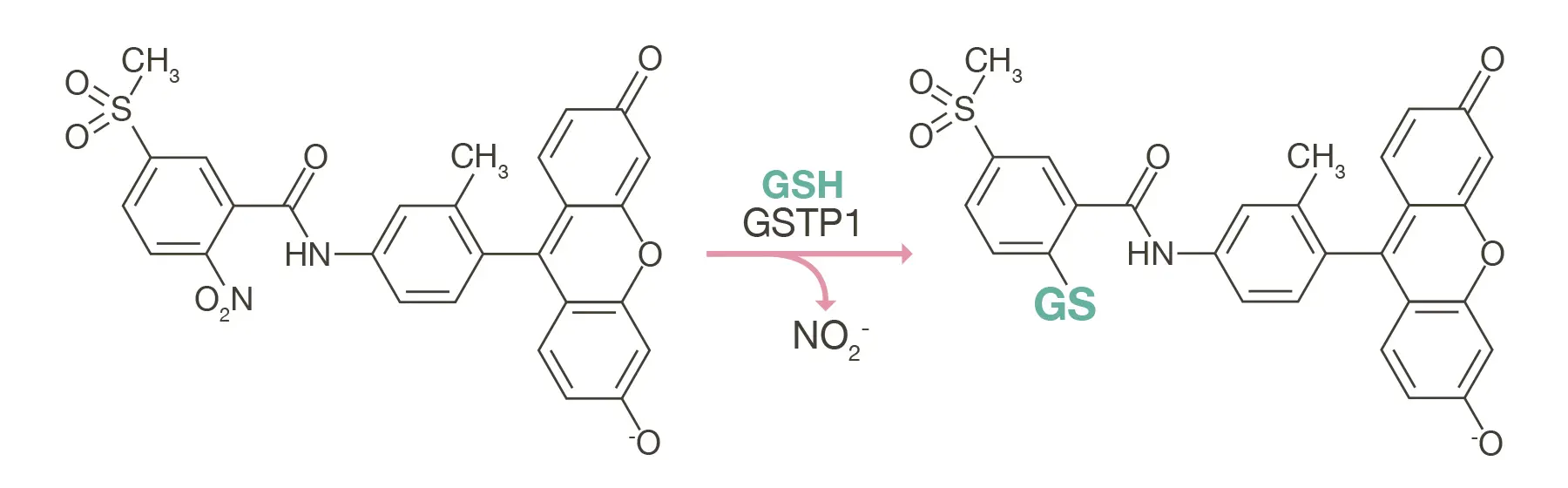
「Ps-TAcは細胞膜を自由に通過できる程度に脂溶性が高いです。細胞内に取り込まれると細胞の中に普遍的に存在するエステラーゼという酵素によって代謝され、Ps-TGができます。Ps-TGはGSTP1の酵素活性によってグルタチオンが付加され、グルタチオン抱合体を形成します。これによって細胞内で緑色蛍光を発するという仕組みです」。効果を確かめるため、藤川准教授らは、この蛍光プローブを使って生細胞でイメージングを行った。「生体内にはがん細胞だけでなく正常細胞も存在しているため、腫瘍マーカーとして使うには、がん細胞と正常細胞を識別する必要があります。そこでがん細胞と、あらかじめ赤色に染色した正常細胞を共培養し、そこにPs-TAcを投与したところ、およそ20分で、がん細胞だけから強い緑色蛍光が検出されました。これによってがん細胞と正常細胞を識別できることも確かめられました」
Ps-TAcは、生きた細胞内のGSTP1活性を特異的に観察できる画期的な蛍光プローブとして、商品化が実現した。がんの治療法や治療薬の研究に寄与する重要なツールの一つになっている。
GSTP1活性を阻害する化合物を探索
抗がん剤耐性の軽減に期待
現在はこの蛍光プローブのさらなる改良にも取り組んでいる。「課題は、グルタチオン抱合体がMRPトランスポーター(多剤耐性タンパクの一種)によって速やかに細胞外に排出されること。あまり速く排出されてしまうと、GSTP1活性を検出できません。つまりがん細胞なのに全く光らないわけです」。現状のCellFluorTM GSTP1ではそれを防ぐためにMRPトランスポーター阻害剤MK571と併用することが推奨されている。藤川准教授は、MRPトランスポーターで細胞の外に排出されない蛍光プローブを開発するべく、分子構造のデザイン・化合物の合成に取り組んでいる。
他方でGSTP1は、抗がん剤などの異物を細胞から追い出し、薬を効きにくくする抗がん剤耐性に重要な酵素でもある。この酵素活性を抑えられれば、抗がん剤などの薬効を高められるとの発想から、GSTP1活性を阻害する化合物の探索も進めている。
目に見えない生体プロセスを可視化する。地道な研究が、未知の生命現象の解明につながっていく。