膵臓のないマウスの体内でiPS細胞から膵臓をつくる
疾病や外傷によって臓器が機能不全に陥り、移植でしか治療する方法のない患者が世界中に数多くいる。それに対し、ドナーの数は圧倒的に不足しており、臓器を作出する新しい方法の開発が課題になってきた。その中にあって、再生医療の新たな活路として有望視されているのが、どんな細胞にも分化できる人工多能性幹細胞(iPS細胞)である。世界中で研究が行われており、すでにiPS細胞から作られた網膜色素上皮シートが治療に用いられるなど、臨床応用が進みつつある。
「iPS細胞から in vitroで細胞を分化する技術は著しく進化していますが、いまだ厚みのある組織を血流のない培養環境で作ることは難しく、三次元の立体構造を持ち、生体と同じ機能を発揮できる臓器をin vitroで人工的に構築できるまでには至っていません」。そう解説する山口智之教授は、in vitroではなく、動物の発生システムを利用し、動物の体内でiPS細胞から「完全な臓器」を作り出す方法を研究している。
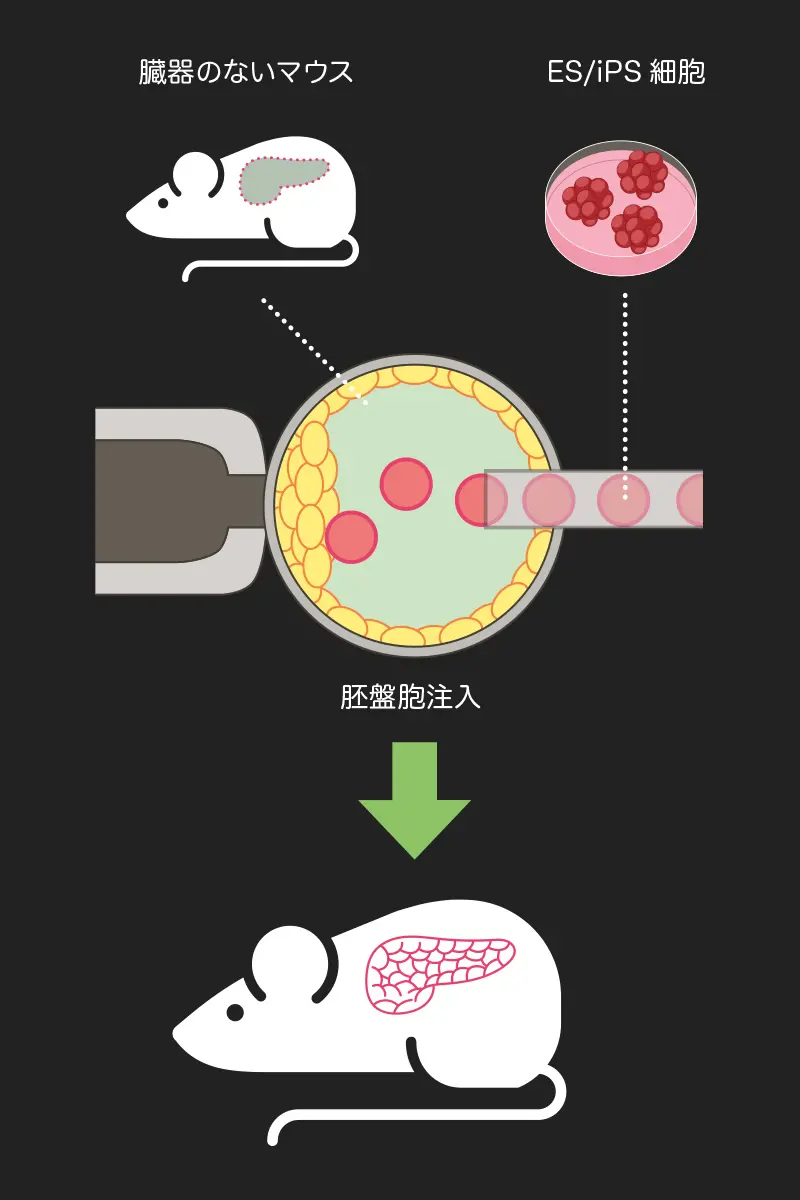
「我々が行っているのは、『胚盤胞補完法』という手法です」と山口教授。試みたのは、遺伝的に膵臓が形成されないマウスの胚盤胞に正常なiPS細胞を注入し、マウスの体内でiPS細胞由来の膵臓を形成するというものだ。
まず野生型マウスと膵臓形成のマスター遺伝子であるPdx1を欠損したキメラマウスを交配し、ヘテロPdx1欠損マウスを作製する。Pdx1は、胎生期の膵臓形成に必須の転写因子で、これが欠損すると、膵臓が形成されない。このヘテロ欠損マウス同士を交配することで、得た完全にPdx1遺伝子が欠損した胚盤胞内に、正常マウスiPS細胞を注入する。胚盤胞とは、受精卵から3日ほど経過し、着床直前にまで成長したものである。これがやがて成体になり、膵臓を作れないはずのPdx1 KOマウスの体内に、正常マウスiPS細胞由来の膵臓を作製することに成功した。「検証の結果、マウス体内に作製された膵臓は、完全にiPS細胞由来であり、形態も機能も正常な膵臓と同じであることが確かめられました」と言う。
膵臓は、血糖値を下げる働きを持つ。血糖値が上がると、膵臓内の膵島にあるβ細胞からインスリンが分泌され、血中のグルコース濃度を下げる仕組みだ。「作製したiPS細胞由来の膵臓からβ細胞を含む膵島を単離し、糖尿病モデルマウスに移植したところ、血糖値が正常値まで下がりました」と山口教授。移植した膵島を除去すると、再び血糖値が急激に上昇。この結果から、膵臓が確かに機能していることが明らかになった。
その後、山口教授らを追従し、世界中で胚盤胞補完法による臓器を作出する試みが行われ、現在までに腎臓や血管・血液、肺、肝臓などが作製されている。「現在も、私たちが開発したこの胚盤胞補完法が、完全な臓器を作出できる唯一の方法です」と言う。
異種動物の体内で臓器作製に成功
「最終目的は、iPS細胞から作った臓器を、臓器機能不全患者の移植治療に用いることです。例えば、ヒトと臓器の大きさがほぼ同じの豚の胚盤胞にヒトiPS細胞を注入し、豚の体内でヒトの臓器を作製することも考えています」と山口教授。だがそれには、ヒト-動物という異種間キメラの体内での臓器作製を可能にする必要がある。
そこで山口教授らが挑戦したのが、ラットの体内にマウスの膵臓を作ることだった。ラットとマウスは、同じネズミ科の動物だが、まったく異なる種であり、染色体数も違えば、体格もラットの方が10倍近く大きい。「先述と同様の方法で膵臓を欠損したPdx1 KOラットの胚盤胞にEGFPで蛍光染色した正常なマウスiPS細胞を注入し、異種間キメラを作製しました。この結果、成体にまでうまく成長する異種間キメララットが得られました」
このキメララットを調べたところ、全体がEGFPの蛍光を発した膵臓が観察され、マウスiPS由来の膵臓が形成されていることが判明した。また耐糖性も正常値を示し、膵臓としての機能を有していることも明らかになった。「キメララットの膵臓のサイズは、同週齢の野生型マウスの膵臓と比べておよそ10倍で、同週齢のラットとほぼ同じでした。これらの結果から、ラットの体内で、マウスiPS細胞がラットの発生機構を経て、正常に機能する膵臓を形成したことが確かめられました」
山口教授らの報告は、動物の体内でヒトiPS細胞からヒトの臓器を作出するという未踏の目標に近づく成果であり、世界に大きなインパクトを与えた。
動物の発生機構を利用し、ヒトiPS細胞から臓器を形成
2019年7月に「動物性集合胚の取扱いに係る関係指針等」が改正され、ヒトiPS細胞を注入した動物胚を動物の子宮に移植し、ヒト-動物キメラを作出する実験が可能になった。
とはいえ「ヒト-動物キメラの作出には、まだまだ高い障壁があります」と山口教授は言う。現在、ヒトiPS細胞が動物の体内でその発生過程と協調しながら臓器を形成していく方法を探求している。世界中で臓器移植を待つ患者を救う「究極の再生医療」の実現に向け、さらに研究を推し進めていく。