泡の粒子を「運び屋」にした
ドラッグデリバリーシステムを開発
ゲノム編集技術の目覚ましい進展に伴い、遺伝子治療の進歩も加速している。しかしこれらの治療技術は、遺伝子治療薬や核酸医薬が疾患部に届いて初めてその真価を発揮できる。遺伝子治療の成否は、薬を標的となる細胞に届ける「運び屋」(キャリア)やドラッグデリバリーシステム(DDS)の開発にかかっていると言っても過言ではないのだ。その中で、「泡」の粒子を「運び屋」とし、超音波を利用して薬を届ける革新的なDDSを開発したのが、根岸洋一教授である。
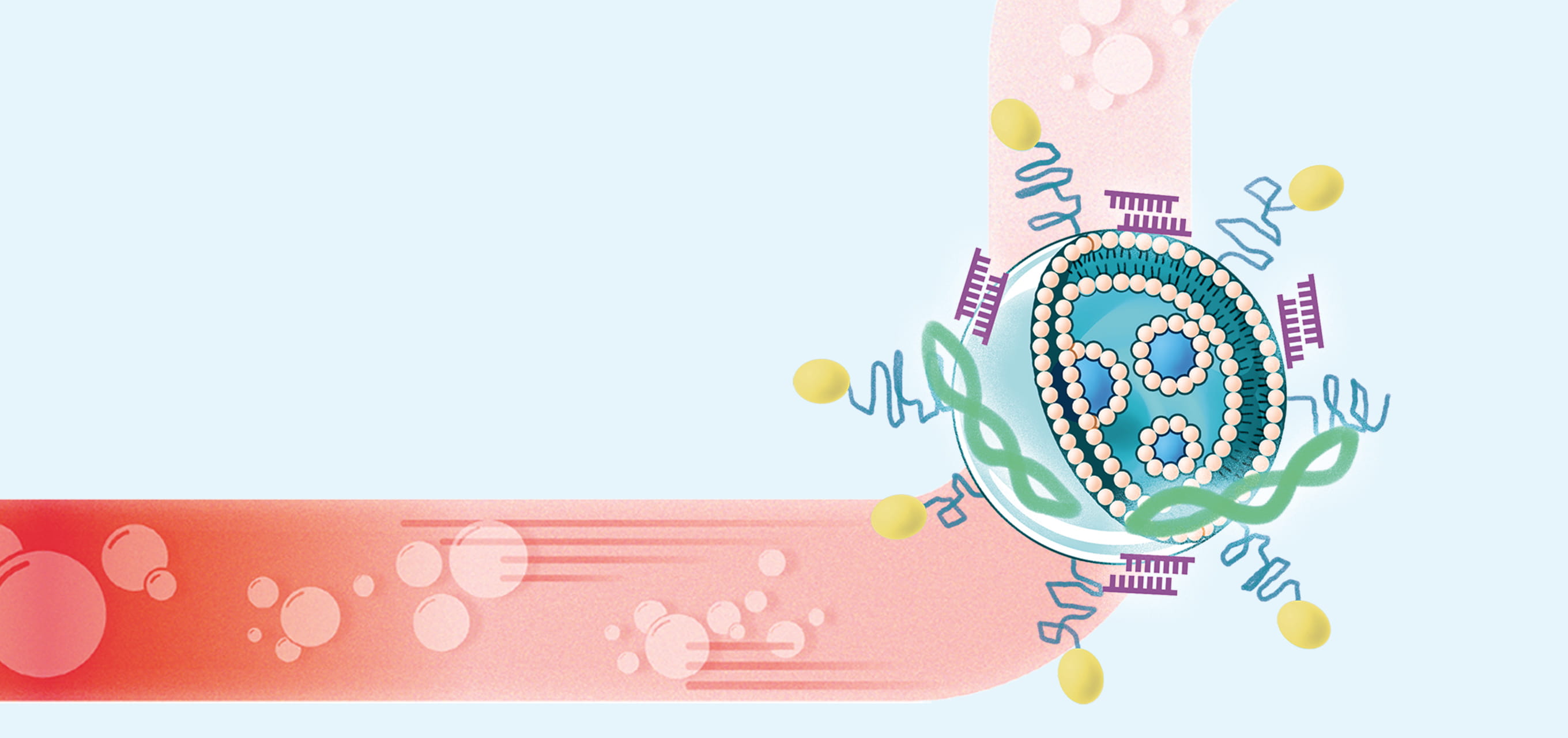
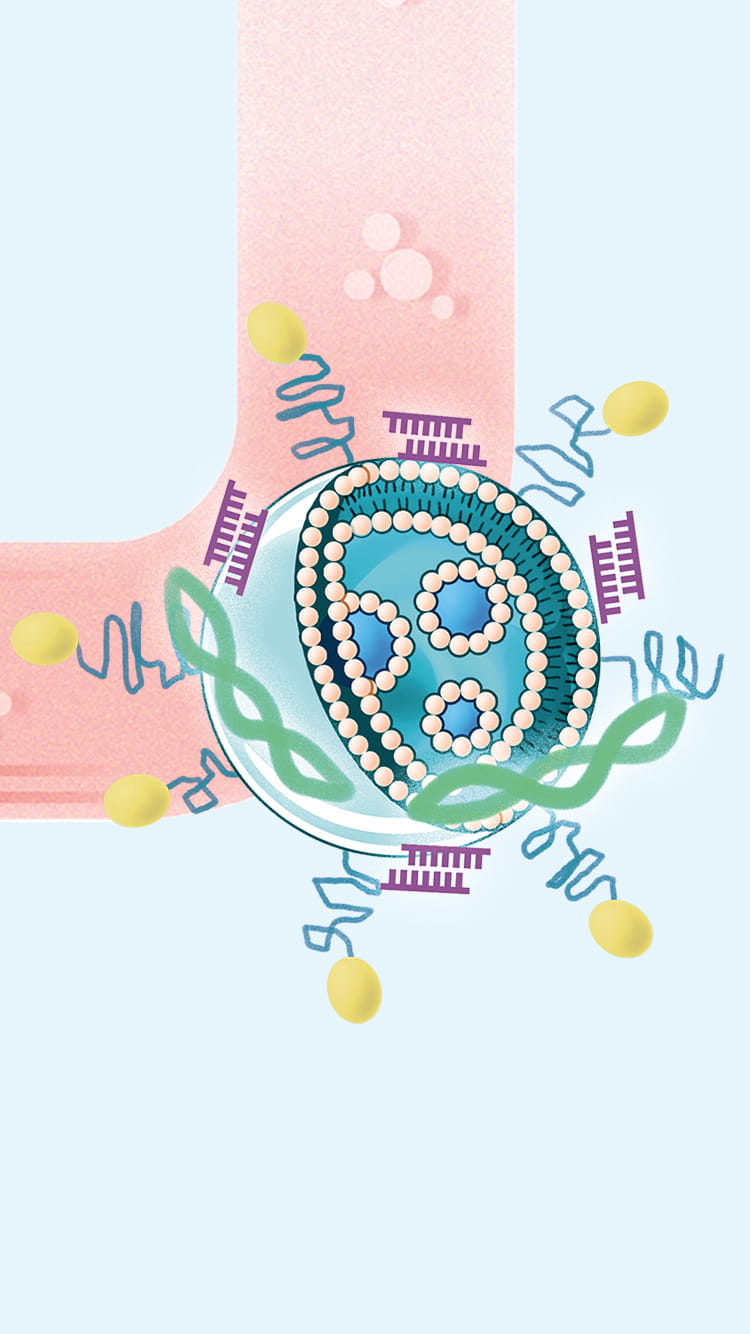
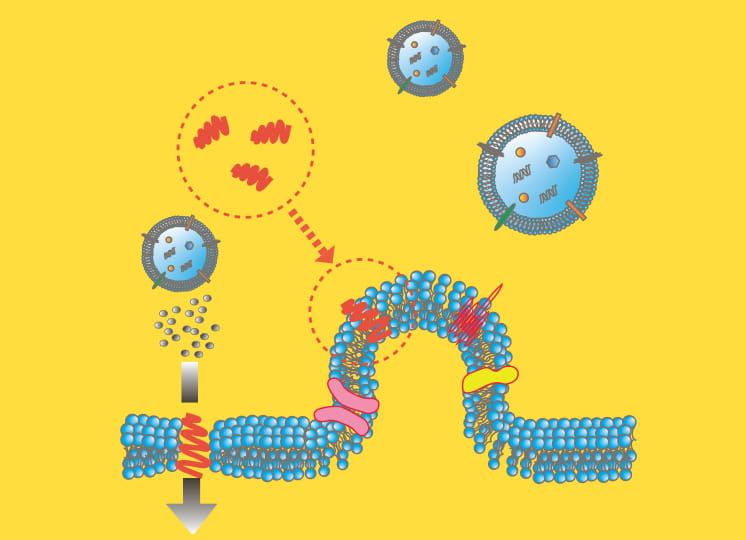
「まずキャリアとして細胞膜の類似成分であるリン脂質を用いて、粒径200~300nmの泡状のナノバブルを作製。この泡の粒子に核酸や遺伝子の治療分子を搭載して血管に注入すると、血流に乗って疾患部の細胞に運ばれます。そこで体外から超音波を照射すれば、バブルが破裂し、衝撃で生まれたマイクロジェット流によって薬が細胞内に導入されるという仕組みです」と説明した根岸教授。超音波は組織へのダメージが少なく低侵襲であることから、これまでもDDSへの応用が検討されてきたものの、既存のキャリアは粒径が4~6μmと大きいことが課題だったという。根岸教授がナノサイズのキャリアの作製に成功したことにより、とうとう遺伝子治療への応用が可能になった。
また根岸教授は、バブルに抗体やペプチドといったアンテナ分子を修飾することで、標的指向性を持ったナノバブルも実現した。「標的細胞に集まったバブルの粒子に微弱な超音波が当たると、音波を跳ね返します。これを利用すれば、超音波造影剤として体外から疾患部を特定する診断イメージングにも活用できます」と言う。さらにナノバブルにアンテナ分子と治療薬を搭載すれば、超音波で患部を特定し、ピンポイントで薬を送り込む、診断と治療を一度に行える革新的なDDSを実現できる。
治療(Therapeutics)と診断(Diagnostics)を組み合わせた「セラノスティクス(Theranostics)」は、患者の負担を軽減し、病気の早期治療を可能にする新しい医療技術として注目されている。ナノサイズでそれを可能にした根岸教授のDDSは世界に大きなインパクトを与えた。